Hóa chất công nghiệp KV. Hà Nội: 0963029988 KV. TP.HCM: 0963029988
Hóa chất công nghiệp KV. Hà Nội: 0963029988 KV. TP.HCM: 0963029988
Hà Nội:
Hóa chất & Thiết bị thí nghiệm KV. Phía Bắc: 0963029988 KV. Phía Nam: 0963029988
Bạn đang tìm kiếm công thức tính pH cho bài tập hóa học hay cần kiểm soát độ pH trong sản xuất, hồ bơi, bể cá? Độ pH là một chỉ số quyền lực, quyết định tính chất của hầu hết dung dịch quanh ta. Trong hướng dẫn toàn diện này, chuyên gia hóa học của VIETCHEM sẽ phân tích tất cả các công thức tính pH từ cơ bản đến nâng cao, kèm theo ví dụ minh họa dễ hiểu và các lưu ý thực tiễn quan trọng mà bạn không thể bỏ qua.

Hiểu một cách đơn giản, pH là chỉ số đo độ axit hay độ kiềm (bazo) của một dung dịch. Về mặt hóa học, pH là một thang đo logarit của nồng độ ion hydro (H⁺) trong dung dịch.
Thang đo pH là một dải số chạy từ 0 đến 14, giúp chúng ta xác định nhanh chóng tính chất của một dung dịch:
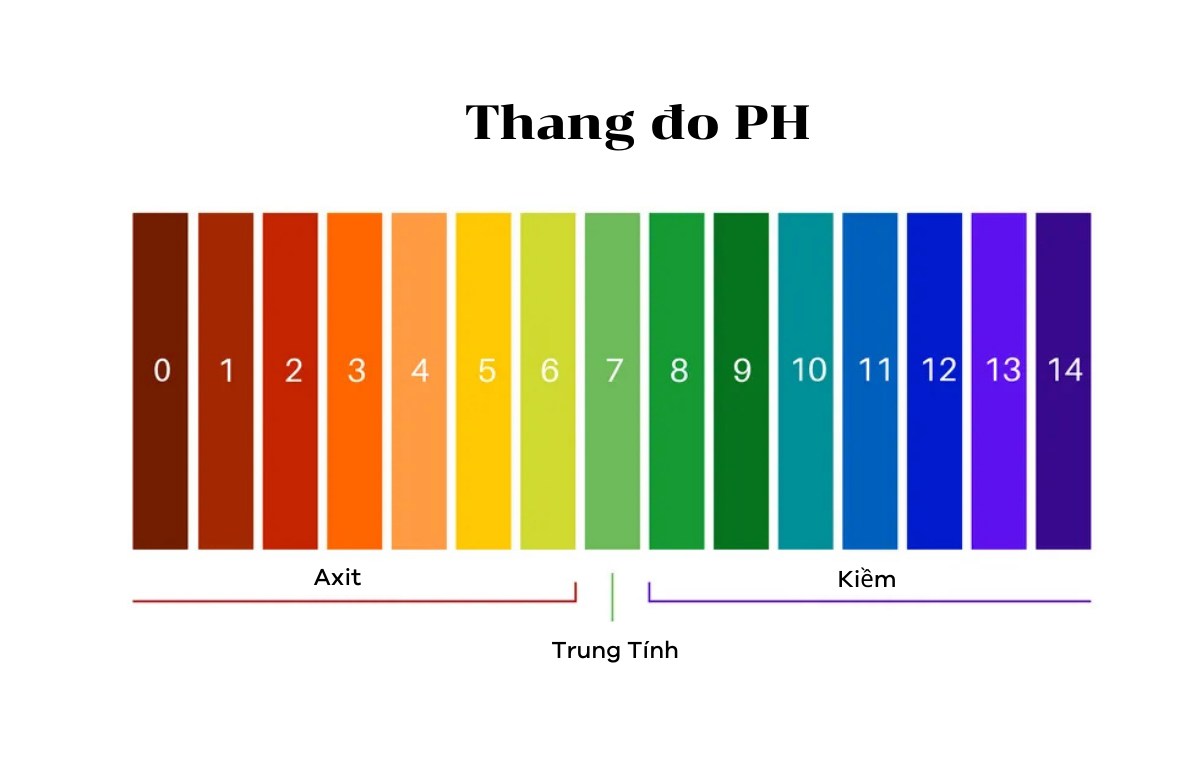
Kiểm soát pH là yếu tố cốt lõi trong vô số lĩnh vực:
Dưới đây là các công thức bạn cần nắm vững, được sắp xếp theo mức độ từ cơ bản đến nâng cao.
Đây là hai công thức nền tảng nhất trong hóa học dung dịch:
pH=−log[H+]
pOH=−log[OH−]
Trong đó:
Mối liên hệ vàng: Ở 25°C, pH và pOH luôn liên kết với nhau qua một hằng số:
pH+pOH=14
Điều này có nghĩa là nếu bạn biết pH, bạn có thể dễ dàng tìm ra pOH và ngược lại.
Axit mạnh và bazo mạnh là các chất điện li mạnh, chúng phân ly hoàn toàn trong nước. Vì vậy, nồng độ ion H⁺ hoặc OH⁻ sẽ bằng chính nồng độ ban đầu của axit hoặc bazo.
Ví dụ: Tính pH của dung dịch HCl 0.01M.
Với Bazo mạnh: [OH⁻] = Cₑ (Cₑ là nồng độ mol của bazo)
Ví dụ: Tính pH của dung dịch NaOH 0.01M.
Vì NaOH là bazơ mạnh, [OH⁻] = 0.01 M = 10⁻² M.
Ta có: pOH = -log(10⁻²) = 2.
Vậy: pH = 14 - pOH = 14 - 2 = 12.

Các phương pháp đo pH
Axit yếu và bazo yếu chỉ phân ly một phần trong nước. Để tính pH, chúng ta cần dùng đến hằng số phân ly axit (Kₐ) hoặc hằng số phân ly bazo (Kₐ).
Dung dịch đệm là dung dịch có khả năng duy trì độ pH gần như không đổi khi thêm một lượng nhỏ axit hoặc bazo. Đây là loại dung dịch cực kỳ quan trọng.
Phương trình Henderson-Hasselbalch:
pH=pKa+log[A−]/[HA]
Trong đó:

Công thức tính pH dung dịch đệm
Tại VIETCHEM, chúng tôi hiểu rằng việc tính toán và kiểm soát pH không chỉ là lý thuyết. Đó là yếu tố quyết định chất lượng sản phẩm và hiệu quả sản xuất. Ví dụ:
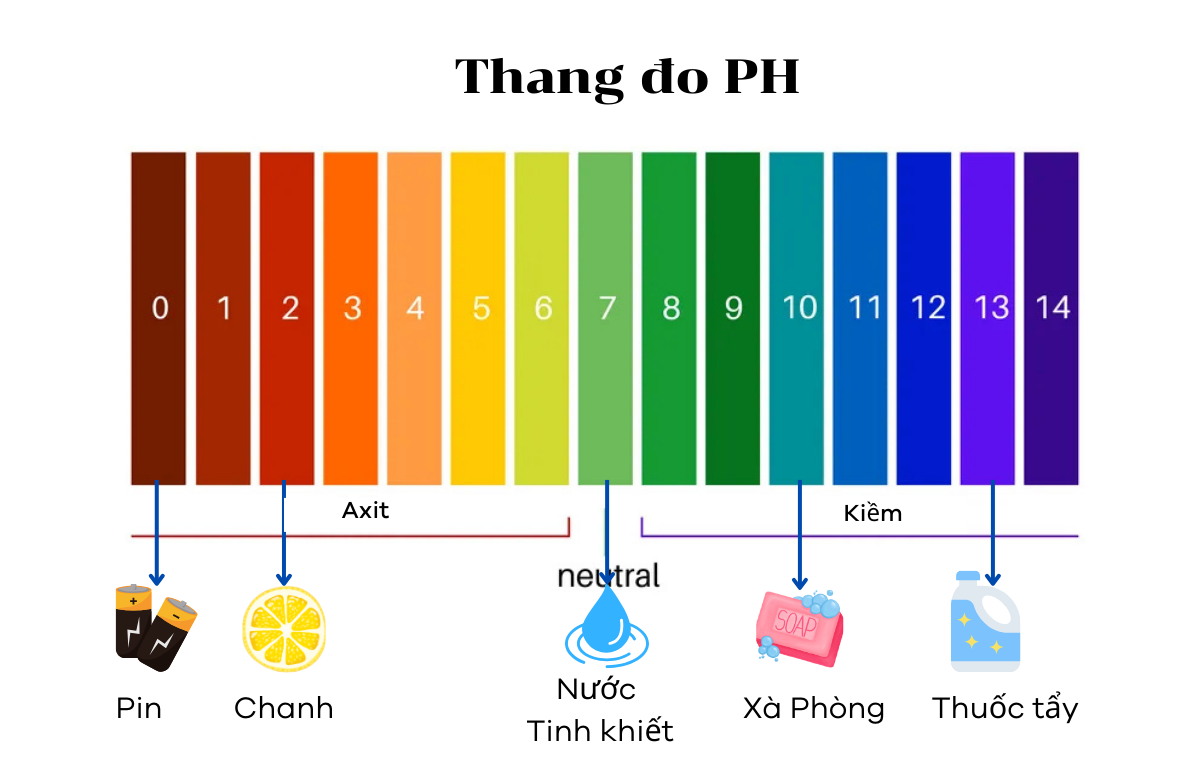
Để dễ hình dung, bạn có thể tham khảo bảng giá trị pH của một số dung dịch quen thuộc trong đời sống.
|
Dung dịch |
Giá trị pH (ước tính) |
|
Axit Ắc quy |
< 1.0 |
|
Dịch vị dạ dày |
1.5 - 3.5 |
|
Nước chanh |
2.4 |
|
Giấm ăn |
2.9 |
|
Cà phê |
5.0 |
|
Sữa tươi |
6.5 |
|
Nước tinh khiết |
7.0 |
|
Máu người |
7.35 - 7.45 |
|
Nước biển |
8.0 |
|
Xà phòng |
9.0 - 10.0 |
|
Amoniac (NH₃) |
11.0 |
|
Thuốc tẩy (Javen) |
12.5 |
|
Xút ăn da (NaOH) |
14.0 |
Sử dụng công thức pH + pOH = 14 (ở 25°C). Nếu bạn có pOH = 3, thì pH = 14 - 3 = 11.
Có hai phương pháp chính:
Nhiệt độ ảnh hưởng đến giá trị pH. Hầu hết các phép tính và thang đo chuẩn đều dựa trên nhiệt độ 25°C. Khi đo lường, cần hiệu chuẩn máy đo pH bằng các dung dịch đệm chuẩn để đảm bảo độ chính xác.
Việc nắm vững các công thức tính pH là kỹ năng thiết yếu cho bất kỳ ai làm việc trong lĩnh vực hóa học, sinh học và các ngành công nghiệp liên quan. Từ những công thức cơ bản đến phương trình Henderson-Hasselbalch phức tạp, mỗi công thức đều mở ra một cánh cửa để hiểu và kiểm soát thế giới hóa học xung quanh chúng ta.
Nếu bạn cần tư vấn về các dung dịch đệm chuẩn, hóa chất công nghiệp, hay các thiết bị đo lường chuyên dụng cho phòng thí nghiệm và nhà máy, hãy liên hệ ngay với VIETCHEM để nhận được giải pháp tối ưu và sự hỗ trợ chuyên nghiệp nhất!
Nguồn tham khảo: Các khái niệm và công thức được đối chiếu với định nghĩa từ Hiệp hội Hóa học Thuần túy và Ứng dụng Quốc tế (IUPAC).
Bài viết liên quan
Khí Amoniac NH3 Có Làm Đổi Màu Quỳ Tím Không? Bản Chất Hóa Học Và Ứng Dụng Thực Tế
0
Hướng dẫn chi tiết cách pha xút vảy NaOH đúng tỷ lệ cho từng ứng dụng từ chuyên gia VIETCHEM. Quy tắc vàng chống bỏng kiềm và cách xử lý khi bị xút ăn da chuẩn y tế.
0
Axit sunfuric đặc (H₂SO₄) là một hóa chất công nghiệp phổ biến nhưng ẩn chứa nguy cơ gây bỏng hóa chất nghiêm trọng nếu thao tác sai kỹ thuật. Trong bài viết này, chuyên gia VIETCHEM với hơn 20 năm kinh nghiệm sẽ hướng dẫn bạn cách pha loãng axit sunfuric đặc an toàn
0
Khám phá chi tiết về Axit Sunfuric đặc H2SO4: Từ tính chất hóa học đặc trưng, phản ứng với kim loại/phi kim đến quy tắc an toàn và cách sơ cứu khi bị bỏng axit.
0

MIỀN BẮC
Hóa chất & Thiết bị thí nghiệm
0826 020 020
sales@labvietchem.com.vn

MIỀN TRUNG
Hóa chất & Thiết bị thí nghiệm
0826 020 020
sales@labvietchem.com.vn

MIỀN NAM
Hóa chất thí nghiệm
0825 250 050
saleadmin808@vietchem.vn

MIỀN NAM
Thiết bị thí nghiệm
0939 154 554
kd201@labvietchem.com.vn

Đinh Phương Thảo
Giám đốc kinh doanh
0963 029 988
sales@hoachat.com.vn

Đào Phương Hoa
Hóa Chất Công Nghiệp
0904 338 331
hoadao@vietchem.com.vn

Lê Thị Mộng Vương
Hóa Chất Công Nghiệp
0964 674 897
kd867@vietchem.vn

Hồ Thị Hoài Thương
Hóa chất và Thiết bị thí nghiệm
096 7609897
kd801@labvietchem.vn

Trần Sĩ Khoa
Hóa Chất Công Nghiệp
0888 851 648
cskh@drtom.vn

Mai Văn Đền
Hóa Chất Công Nghiệp
0888 337 431
cskh@drtom.vn

Phạm Văn Trung
Hóa Chất Công Nghiệp
0918 986 544 0328.522.089
kd805@vietchem.vn

Kiều Nhật Linh
Hóa Chất Công Nghiệp
0325909968
CTY.sales470@vietchem.vn
Gửi bình luận mới
Gửi bình luận