Hóa chất công nghiệp KV. Hà Nội: 0963029988 KV. TP.HCM: 0963029988
Hóa chất công nghiệp KV. Hà Nội: 0963029988 KV. TP.HCM: 0963029988
Hà Nội:
Hóa chất & Thiết bị thí nghiệm KV. Phía Bắc: 0963029988 KV. Phía Nam: 0963029988
NaHCO3 (Natri Bicarbonat) và NaOH (Natri Hydroxit) là hai hợp chất hóa học quen thuộc với nhiều ứng dụng trong đời sống và công nghiệp. Khi kết hợp, chúng tạo nên một phản ứng thú vị với nhiều khía cạnh cần được tìm hiểu sâu. Bài viết này, được biên soạn bởi các chuyên gia hóa học của VIETCHEM, sẽ cung cấp cho bạn cái nhìn toàn diện về phản ứng NaHCO3 + NaOH, từ cơ chế phản ứng, các dạng phương trình cho đến những ứng dụng quan trọng trong thực tế.
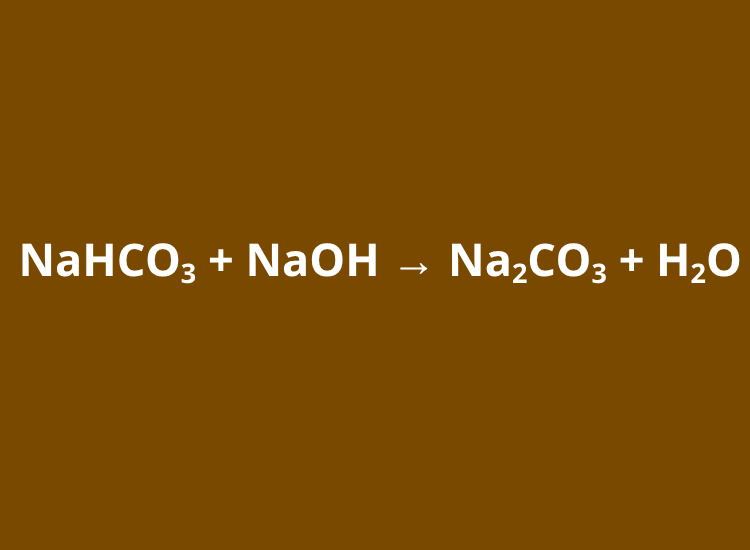
Phương Trình Phản Ứng Và Cân Bằng Phương Trình Phản Ứng
NaHCO3 + NaOH → Na2CO3 + H2O
Giải thích:
Natri Bicarbonat hay còn gọi là Sodium Bicarbonate hoặc baking soda, là một hợp chất hóa học vô cơ có nhiều ứng dụng.
2NaHCO3 (to) → Na2CO3 + H2O + CO2↑
Natri Hydroxit hay còn gọi là Sodium Hydroxide, xút ăn da, hoặc caustic soda, là một bazơ mạnh không thể thiếu trong nhiều ngành công nghiệp.
| Thuộc tính | Mô tả chi tiết |
| Trạng thái | Chất rắn màu trắng, thường tồn tại dưới dạng vảy, hạt, hoặc viên. |
| Màu sắc | Trắng. |
| Độ tan | Tan rất tốt trong nước, giải phóng lượng nhiệt lớn (tỏa nhiệt mạnh). |
| Tính hút ẩm | Có khả năng hút ẩm mạnh mẽ từ không khí, dễ bị chảy rữa (hóa lỏng do hấp thụ nước). |

Natri hiđroxit (NaOH) là một bazơ mạnh, khi hòa tan trong nước sẽ phân ly hoàn toàn thành ion OH-. Một số phản ứng phổ biến của NaOH
Phản ứng giữa NaHCO3 và NaOH là một phản ứng trung hòa điển hình giữa một muối axit (NaHCO3, với tính axit yếu của ion HCO3-) và một bazơ mạnh (NaOH).
Khi hòa tan vào nước, NaOH phân ly hoàn toàn thành ion Na+ và OH-. NaHCO3 cũng phân ly tạo ra các ion Na+ và HCO3-. Điểm cốt lõi của phản ứng NaHCO3 + NaOH nằm ở sự tương tác của ion hydroxit (OH-) từ NaOH với ion bicacbonat (HCO3-) từ NaHCO3.
Ion bicacbonat (HCO3-) mang tính lưỡng tính, nhưng trong môi trường kiềm mạnh của NaOH, nó sẽ thể hiện tính axit yếu và nhường proton (H+) cho ion hydroxit (OH-).
Về bản chất, đây là một phản ứng axit-bazơ (phản ứng trung hòa) giữa axit yếu HCO3- (đóng vai trò là axit Bronsted-Lowry) và bazơ mạnh OH-.
Sự tương tác này tạo ra ion cacbonat (CO32-) và phân tử nước (H2O). Ion Na+ đóng vai trò là "ion khán giả" và không tham gia trực tiếp vào phản ứng hóa học.
Có ba cách chính để biểu diễn phản ứng NaHCO3 + NaOH, mỗi cách mang một ý nghĩa riêng trong hóa học.
Đây là dạng phương trình cơ bản nhất, thể hiện đầy đủ công thức hóa học của các chất tham gia và sản phẩm.
NaHCO3 + NaOH → Na2CO3 + H2O
Để dễ hình dung hơn, dưới đây là bảng tóm tắt các chất trong phản ứng:
| Chất phản ứng | Công thức hóa học | Trạng thái (trong dd) | Vai trò |
| Natri Bicarbonat | NaHCO3 | Dung dịch | Muối axit lưỡng tính |
| Natri Hydroxit | NaOH | Dung dịch | Bazơ mạnh |
| Sản phẩm | Công thức hóa học | Trạng thái (trong dd) | Tính chất |
| Natri Cacbonat | Na2CO3 | Dung dịch | Muối trung hòa |
| Nước | H2O | Lỏng | Dung môi |
Phương trình ion đầy đủ thể hiện tất cả các ion có mặt trong dung dịch, bao gồm cả các ion tham gia phản ứng và các ion "khán giả".
Na+ + HCO3- + Na+ + OH- → 2Na+ + CO32- + H2O
Phương trình ion rút gọn chỉ thể hiện các ion hoặc phân tử thực sự tham gia vào quá trình biến đổi hóa học, loại bỏ các ion "không tham gia".
HCO3- + OH- → CO32- + H2O
Mặc dù phản ứng NaHCO3 + NaOH diễn ra dễ dàng, nhưng việc hiểu các yếu tố ảnh hưởng và lưu ý quan trọng sẽ giúp chúng ta kiểm soát và áp dụng phản ứng hiệu quả hơn.
Phản ứng giữa NaHCO3 và NaOH không chỉ là một kiến thức hóa học cơ bản đồng thời được ứng dụng rộng rãi trong nhiều lĩnh vực công nghiệp và đời sống hằng ngày.

Ứng dụng thực tiễn của phản ứng NaHCO3 + NaOH
Để củng cố kiến thức về phản ứng NaHCO3 + NaOH, chúng ta hãy cùng thực hiện một số bài tập vận dụng.
Bài tập 1: Phương trình hóa học nào sau đây biểu diễn đúng phản ứng giữa Natri Bicarbonat và Natri Hydroxit?
Đáp án: A
Lời giải và Giải thích: Phản ứng giữa NaHCO3 và NaOH là một phản ứng trung hòa giữa muối axit yếu (NaHCO3) và bazơ mạnh (NaOH). Ion bicacbonat (HCO3-) sẽ nhường proton (H+) cho ion hydroxit (OH-) để tạo thành ion cacbonat (CO32-) và nước (H2O). Phương trình cân bằng là 1:1 tỉ lệ mol giữa NaHCO3 và NaOH. NaHCO3 + NaOH → Na2CO3 + H2O
Bài tập 2: Khi cho dung dịch NaOH vào dung dịch NaHCO3, hiện tượng nào sau đây có thể quan sát được bằng mắt thường?
Đáp án: D
Lời giải và Giải thích: Phản ứng NaHCO3 + NaOH tạo ra Natri Cacbonat (Na2CO3) và nước (H2O). Cả NaHCO3, NaOH và Na2CO3 đều là các chất tan tốt trong nước, tạo thành dung dịch trong suốt. Phản ứng này không sinh ra chất khí hay chất kết tủa, cũng không có sự thay đổi màu sắc rõ rệt của dung dịch. Do đó, bằng mắt thường, chúng ta sẽ không thấy hiện tượng gì đặc biệt.
Bài tập 3: Phương trình ion rút gọn của phản ứng NaHCO3 + NaOH là:
Đáp án: B
Lời giải và Giải thích: Phương trình ion rút gọn chỉ biểu diễn các ion hoặc phân tử thực sự tham gia vào quá trình phản ứng hóa học. Trong phản ứng NaHCO3 với NaOH, ion Na+ là ion "khán giả" (không tham gia trực tiếp vào phản ứng). Ion bicacbonat (HCO3-) phản ứng với ion hydroxit (OH-) để tạo thành ion cacbonat (CO32-) và nước (H2O). HCO3- (aq) + OH- (aq) → CO32- (aq) + H2O (l)
Bài tập 4: Cho 0,2 mol NaHCO3 tác dụng vừa đủ với dung dịch NaOH. Vậy lượng NaOH đã phản ứng trong quá trình là bao nhiêu gam? (Biết Na=23, O=16, H=1)
Đáp án: A
Lời giải và Giải thích: Phương trình phản ứng: NaHCO3 + NaOH → Na2CO3 + H2O. Theo phương trình, tỉ lệ mol NaHCO3 : NaOH là 1:1. Số mol NaOH đã phản ứng = Số mol NaHCO3 = 0,2 mol. Khối lượng mol của NaOH được tính bằng: 23 (Na) + 16 (O) + 1 (H) = 40 g/mol. Khối lượng NaOH đã phản ứng = 0,2 mol × 40 g/mol = 8 gam.
Bài tập 5: Hòa tan 21,2 gam Na2CO3 vào nước. Hỏi cần bao nhiêu mol NaOH để phản ứng hết với lượng NaHCO3 thu được khi cho dung dịch này tác dụng với một lượng CO2 dư? (Biết Na=23, C=12, O=16)
Đáp án: C
Lời giải và Giải thích: Đề bài yêu cầu số mol NaOH để phản ứng với NaHCO3 được tạo ra từ Na2CO3 và CO2 dư.
Ca(OH)2 có thể tạo kết tủa CaCO3, nhưng Ca(OH)2 là một bazơ, có thể phản ứng với cả NaHCO3 dư hoặc CO2 nếu có, khiến việc nhận biết không rõ ràng bằng HCl.
Với hơn 20 năm kinh nghiệm trong lĩnh vực kinh doanh và cung ứng hóa chất tại Việt Nam, VIETCHEM tự hào là đối tác tin cậy của hàng ngàn doanh nghiệp và phòng thí nghiệm trên khắp cả nước. Chúng tôi không chỉ cung cấp đa dạng các loại hóa chất công nghiệp, hóa chất thí nghiệm chất lượng cao, bao gồm cả NaOH và NaHCO3 với độ tinh khiết đảm bảo, mà còn cam kết mang đến những giải pháp hóa học toàn diện, an toàn và hiệu quả.
Chúng tôi hiểu rằng, kiến thức chuyên sâu và sự minh bạch về sản phẩm là yếu tố cốt lõi tạo nên sự tin cậy. Đội ngũ chuyên gia của VIETCHEM luôn sẵn sàng tư vấn, hỗ trợ quý khách hàng trong việc lựa chọn hóa chất, hướng dẫn sử dụng an toàn và tối ưu hóa các quy trình sản xuất.
Nếu quý khách hàng có nhu cầu về NaOH, NaHCO3 hay bất kỳ loại hóa chất nào khác, đừng ngần ngại liên hệ với VIETCHEM để được tư vấn và hỗ trợ tốt nhất:
Phản ứng giữa NaHCO3 và NaOH là một minh chứng rõ ràng về sự tương tác hóa học cơ bản nhưng lại mang nhiều ý nghĩa thực tiễn. Từ việc cân bằng phương trình NaHCO3 + NaOH đến việc hiểu sâu sắc cơ chế ion và ứng dụng trong các ngành công nghiệp quan trọng như sản xuất hóa chất, xử lý nước hay tẩy rửa, phản ứng này đóng góp không nhỏ vào đời sống và sự phát triển công nghiệp.
VIETCHEM hy vọng bài viết này đã cung cấp cho bạn cái nhìn toàn diện và hữu ích về chủ đề này. Với cam kết về chất lượng và chuyên môn, chúng tôi luôn là đối tác đáng tin cậy của bạn trong mọi nhu cầu về hóa chất.
Bài viết liên quan
Axit sunfuric (H2SO4) được mệnh danh là "ông vua của các loại hóa chất" nhờ vai trò không thể thay thế trong nền kinh tế toàn cầu. Mức độ tiêu thụ hóa chất này thường được dùng làm thước đo cho sức mạnh công nghiệp của một quốc gia. Vậy thực tế axit sunfuric dùng để làm gì? Tại sao trong acquy chì chứa dung dịch axit sunfuric? Với hơn 20 năm kinh nghiệm trong ngành hóa chất, VIETCHEM sẽ giải đáp chi tiết các công dụng của axit sunfuric, từ quy mô phòng thí nghiệm đến các khu công nghiệp khổng lồ, đồng thời cung cấp những tiêu chuẩn an toàn khắt khe nhất.
0
Axit Sulfuric (H2SO4) là hóa chất quan trọng nhưng tiềm ẩn nguy hiểm cao, đòi hỏi đơn vị cung ứng phải có năng lực chuyên môn và hệ thống vận chuyển chuyên dụng. Bạn đang tìm địa chỉ bán lẻ axit sunfuric tại Hà Nội chất lượng, giá tốt và có đầy đủ giấy tờ kiểm định? Bài viết này sẽ cung cấp bảng giá axit sunfuric 98 mới nhất và danh sách các đơn vị cung ứng uy tín, đảm bảo an toàn vận chuyển, giúp bạn trả lời câu hỏi axit sunfuric mua ở đâu là tốt nhất.
0
Hiệu suất phản ứng không chỉ là một con số khô khan trong các bài kiểm tra hóa học, mà nó chính là "chìa khóa vàng" quyết định trực tiếp đến lợi nhuận, chi phí và sự thành công trong quy trình sản xuất hóa chất công nghiệp.
0

MIỀN BẮC
Hóa chất & Thiết bị thí nghiệm
0826 020 020
sales@labvietchem.com.vn

MIỀN TRUNG
Hóa chất & Thiết bị thí nghiệm
0826 020 020
sales@labvietchem.com.vn

MIỀN NAM
Hóa chất thí nghiệm
0825 250 050
saleadmin808@vietchem.vn

MIỀN NAM
Thiết bị thí nghiệm
0939 154 554
kd201@labvietchem.com.vn

Đinh Phương Thảo
Giám đốc kinh doanh
0963 029 988
sales@hoachat.com.vn

Tống Đức Nhuận
Hóa Chất Công Nghiệp
0915 866 828
sales468@vietchem.vn

Lê Thị Mộng Vương
Hóa Chất Công Nghiệp
0964 674 897
kd867@vietchem.vn

Hồ Thị Hoài Thương
Hóa chất và Thiết bị thí nghiệm
096 7609897
kd801@labvietchem.vn

Trần Sĩ Khoa
Hóa Chất Công Nghiệp
0888 851 648
cskh@drtom.vn

Mai Văn Đền
Hóa Chất Công Nghiệp
0888 337 431
cskh@drtom.vn

Phạm Văn Trung
Hóa Chất Công Nghiệp
0918 986 544 0328.522.089
kd805@vietchem.vn

Kiều Nhật Linh
Hóa Chất Công Nghiệp
0325909968
CTY.sales470@vietchem.vn
Gửi bình luận mới
Gửi bình luận